精准的亚细胞递送是实现高效肿瘤治疗的关键前提,尤其是针对以细胞核为主要作用靶点的化疗药物,其治疗效果在很大程度上取决于能否跨越多重细胞内屏障并实现高效入核。然而在实际应用中,药物从细胞外进入细胞后,往往受到内吞体/溶酶体膜及核膜等结构性屏障的严格限制,导致细胞核内药物累积不足,从而显著削弱治疗效果。为克服上述障碍,近年来研究者提出了多种亚细胞递送策略,如引入核定位信号或细胞穿膜肽等,但这些方法普遍存在结构可控性差、体内稳定性不足以及潜在安全风险等问题,严重制约了其在精准肿瘤治疗中的进一步应用。因此,发展一种具有良好生物相容性、可精确调控且安全的核靶向递送新策略,仍然是纳米医学领域亟待解决的核心科学问题。在此背景下,刺激响应型超分子纳米体系因其可通过外源信号实现按需激活和精准调控而受到广泛关注。特别是光响应体系,具有非侵入性、时空分辨率高等独特优势,为突破亚细胞递送瓶颈提供了新的研究契机。然而,如何在不引入复杂生物修饰的前提下,克服细胞内屏障结构并精准控制药物向细胞核转运,仍缺乏明确的设计策略和机制认知。
近年来,课题组围绕光控药物递送及其抗肿瘤效应开展了一系列研究(Nano Today, 2025, 62, 102727;Adv Mater, 202537, e2411515; Nano Lett, 2024, 24, 12239; Nat Commun, 2023, 14, 2498; Adv Mater, 2023, 35, 2210201; J Control Release, 2022, 350, 761; Adv Mater, 2021, 33, 2004225; Adv Mater, 2021, 33, 2100795)。在此基础上,课题组构建了一种光响应性前药超分子组装体系,通过将可光裂解的化疗前药聚合物与两亲性光敏分子协同组装,实现了在光照激活下药物释放与亚细胞递送过程的高度协同调控。该体系结构在特定光刺激下可高效产生单线态氧,触发前药键断裂并诱导溶酶体膜破裂,从而显著促进药物的释放及由溶酶体向细胞质的转运。且产生的单线态氧还可介导核膜脂质过氧化及核纤层蛋白Lamin B1下调,主动重塑核膜结构并显著提高核膜通透性,从而加速化疗药物由细胞质向细胞核的跨膜转运,实现药物在细胞核内的高效富集(图1),在难治性乳腺癌模型中表现出显著增强的抗肿瘤疗效。该工作以“Photo-responsive polyprodrug supramolecular assemblies with self-accelerated subcellular delivery for synergistic photochemotherapy”为题,发表于Science Bulletin杂志上。Science Bulletin是由中国科学院和国家自然科学基金委员会共同主办、Elsevier出版社发行的综合性学术期刊,2025年影响因子为21.1。
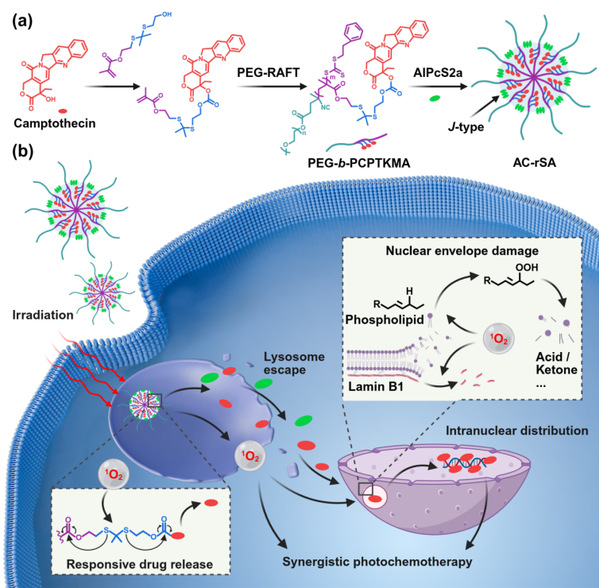
图1. 光响应超分子纳米组装体实现抗肿瘤药物高效细胞核递送
该研究首先将可光裂解的化疗前药聚合物(PEG-b-PCPTKMA)与两亲性光敏分子(AlPcS2a)组装,制得尺寸为29.7 nm的光响应超分子纳米组装体(AC-rSA)(图2a),其在近红外光照射下产生大量单线态氧(图2b),诱导化疗药物CPT的可控释放(图2c);胞内活性氧可促进核膜脂质过氧化及核纤层蛋白Lamin B1下调(图2d-g),提升细胞核膜通透性,加速核内化疗药物的富集(图2h和i),高效抑制肿瘤生长及转移(图2j和k)。
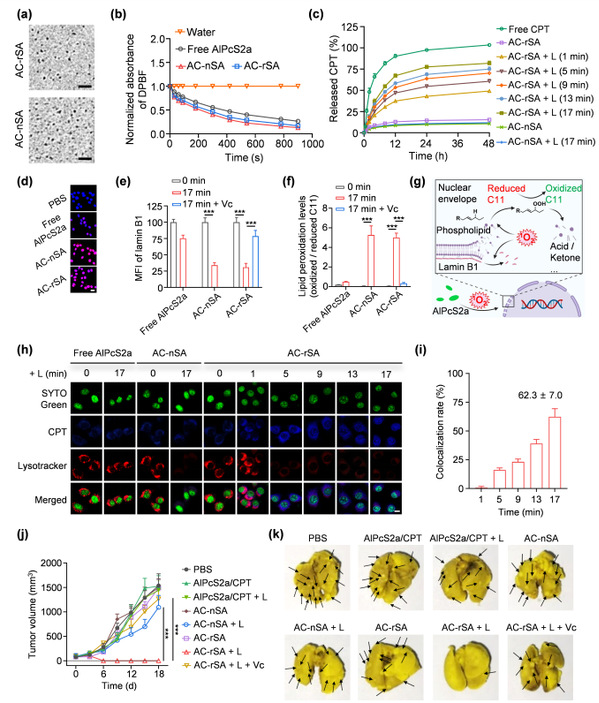
图2. (a)纳米组装体的透射电镜图,标尺=200 nm;(b)以DPBF为探针测得的纳米组装体产生单线态氧的情况;(c)纳米组装体在不同光照条件下释放CPT的行为;(d)纳米组装体在细胞内产生活性氧的共聚焦显微镜图像,标尺=20 μm;(e)纳米组装体在不同光照条件下对lamin B1表达的影响;(f)纳米组装体在不同光照条件下诱导脂质过氧化的能力;(g)纳米组装体在光照条件下产生单线态氧,诱导脂质过氧化及核纤层蛋白Lamin B1下调,主动重塑核膜结构并显著提高核膜通透性;(h)不同光照条件下,纳米组装体递送的CPT在溶酶体和细胞核的分布情况,标尺=10 μm;(i)CPT与细胞核共定位率的统计;纳米组装体治疗4T1肿瘤模型后肿瘤生长曲线(j)及肺转移图像(k)
课题组博士生刘明、赵振铎和博士后李明为共同第一作者,陈华兵教授、邓益斌教授、唐永安副教授、暨南大学赵宇亮院士与西安交通大学葛治伸教授为共同通讯作者。该研究得到了国家自然科学基金、科技部重点研发计划课题、以及江苏高校优势学科建设工程等项目的资助。
论文信息:https://doi.org/10.1016/j.scib.2026.01.002
Ming Liu,† Zhenduo Zhao,† Ming Li,† Yitian Chen, Yicheng Wang, Xuehua Lin, Xinyu Wang, Qinghao Zhou,Zhishen Ge,* Yongan Tang,* Yibin Deng,* Yuliang Zhao,*Huabing Chen*Photo-responsive polyprodrug supramolecular assemblies with self-accelerated subcellular delivery for synergistic photochemotherapy.Science Bulletin, 2026, DOI: 10.1016/j.scib.2026.01.002.
